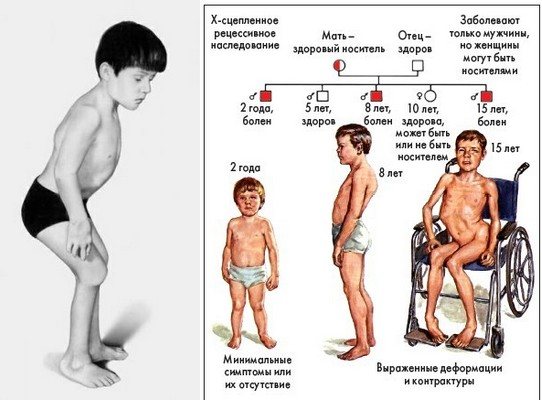
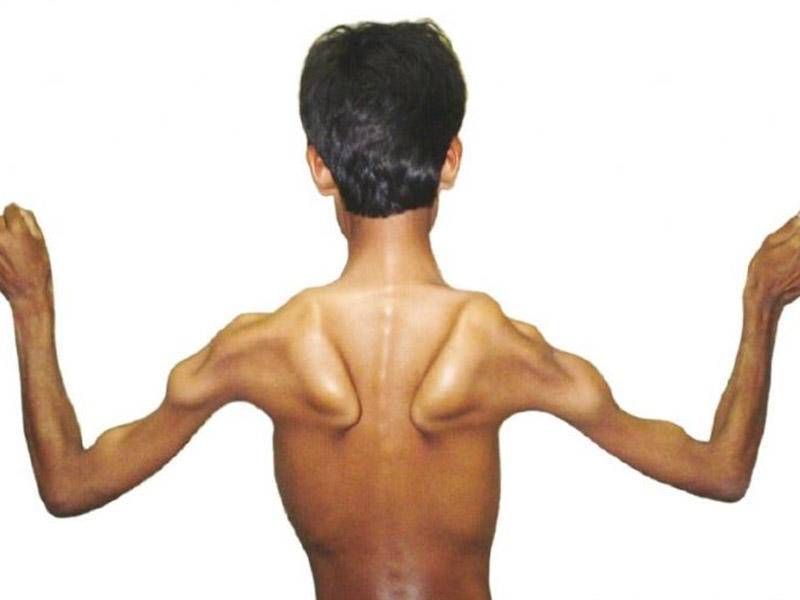
Диагностика
Для постановки точного диагноза врачу, наблюдающему ребенка необходимо:
- Составить семейный анамнез, выявить случаи заболевания в семье пациента (если таковые имеются).
- Провести электромиографию для того, чтобы определить электрическую проводимость мышечных тканей.
- Сделать биопсию для выявления мутировавшего гена.
- Ферментный анализ крови (при отсутствии травм повышение фермента креатинина сигнализирует о наличии патологических процессов в организме).
- Генетический анализ для выявления мутационных процессов, определения их типа.
Рекомендации по лечению гипоспадии у мальчиков вы найдете на нашем сайте.
Диагностика дистрофии у детей
Диагноз и дифференциальная диагностика дистрофии
Диагноз дистрофии основывается на следующих клинических симптомах:
- снижение тургора тканей;
- последовательное исчезновение или уменьшение толщины подкожной жировой клетчатки на животе, конечностях, лице, а также избыточное и неравномерное ее отложение, отставание массы тела от его длины и других возрастных параметров;
- снижение порога толерантности к пище и сопротивляемости к инфекционным и другим воздействиям внешней среды.
Диагноз должен отражать вид дистрофии, время возникновения по отношению к моменту рождения; при наличии гипотрофии – ее степень и этиологическую принадлежность; периоды развития – начальный, прогрессирования, реконвалесценции.
- Дистрофию sui generis отличают от вторичных дистрофий, вызванных пороками развития желудочно-кишечного тракта и других органов, наследственной патологией, органическими и функциональными поражениями центральной нервной системы, эндокринными заболеваниями, о которых нужно думать во всех случаях тяжелой гипотрофии (II – III степени), не поддающейся лечению, а также паратрофии и ожирения, особенно сочетающихся со значительным отставанием психомоторного развития.
- Гипостатуру дифференцируют от заболеваний, сопровождающихся резким отставанием в физическом развитии, прежде всего нанизма, а также физиологического субнанизма, обусловленного особенностями семейного, национального или расового характера.
- Непропорциональный нанизм, вызванный ахондроплазией, врожденной ломкостью костей, тубулопатиями, отличается от гипостатуры грубой патологией скелета, которую невозможно объяснить сопутствующим дистрофии подостротекущим рахитом. Рентгенограммы костей и отклонения от нормы показателей фосфорно-кальциевого обмена позволяют исключить эти заболевания.
- Пропорциональный нанизм обусловлен поражением гипофиза или тяжелой врожденной патологией сердечно-сосудистой и дыхательной систем. Развивается обычно в более старшем возрасте и редко проявляется при рождении. Затруднения возникают при дифференциальной диагностике от примордиального (простого или первичного) нанизма, обусловленного нечувствительностью тканей организма к гормону роста. Низкие показатели массы и длины тела отмечаются уже при рождении. В дальнейшем прибавка в росте крайне незначительна. В крови увеличено содержание гормона роста. Отсутствуют клинические и лабораторные признаки дистрофии.
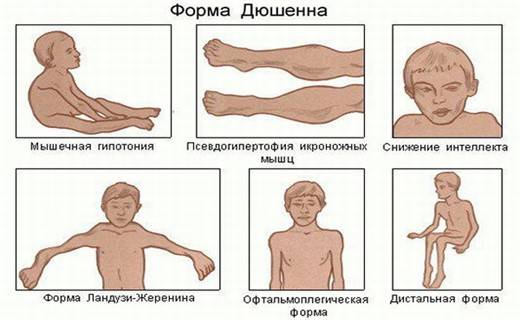
Методы лечения
Терапевтические методы для лечения дистрофии мышц различны, выбор того или иного из них осуществляется на основании диагностических данных, клинических проявлений патологии.
На сегодняшний день применяются медикаментозные способы лечения, методы физиотерапии, использование специальных ортопедических инструментов.
Медикаментозное
Наименование препарата | Особенности применения |
Преднизон | Дозировка и курс приема определяются интенсивностью симптомов заболевания, однако, не рекомендуется употреблять более 0.1 мг. средства в сутки. При продолжительном приеме могут возникать побочные эффекты, такие как отечность, повышение АД. Для устранения этих проявлений рекомендуется соблюдать специальный режим питания (употреблять пищу богатую содержанием солей калия, белковых элементов), принимать препараты анаболитической группы. Существует ряд противопоказаний. Нельзя принимать средство в период беременности и лактации, при заболеваниях сердца, органов ЖКТ. |
Метиландростендиол | Препарат, нормализующий обменные процессы в организме. Не рекомендуется принимать при заболеваниях печени, аллергических реакциях, онкологических опухолях, сахарном диабете. Курс приема 2-4 недели. |
Дифенин | Препарат способствует снятию спазма мышечной ткани. Назначается в дозировке по 0.025 г. 2 раза в день для детей до 5 лет; По 0.1г. 4 раза в день для детей более старшего возраста. Противопоказания: индивидуальная непереносимость компонентов препарата. |
Карбамазепин | Оказывает общеукрепляющее, поддерживающее действие на мышечную ткань организма ребенка. Дозировка назначается индивидуально, в зависимости от степени развития патологии. Противопоказания: аллергические реакции, эпилепсии, заболевания сердца. |
Физиотерапевтические
Для укрепления мышечной ткани необходимо регулярно делать укрепляющую гимнастику – комплекс упражнений, разработанных врачом в зависимости от состояния организма пациента, его возраста, степени развития заболевания и физических возможностей ребенка.
Упражнения должны быть умеренными, ребенку необходимо избегать переутомления, чрезмерной физической активности.
Широко применяют и массажные техники. Для массажа используют максимально щадящие массажные движения. Это должны быть поглаживания, легкие растирания и разминания.
Прикосновения должны быть легкими, осторожными, чтобы не травмировать кожу и мышечную ткань ребенка. Проводить процедуру массажа необходимо ежедневно, лучше всего, если это будет делать специалист (со временем родители могут обучиться технике лечебного массажа самостоятельно).
Дыхательная гимнастика позволяет ребенку расслабиться, насытить клетки тканей организма кислородом, что способствует восстановлению обменных процессов, укреплению и регенерации тканей.
Ортопедические приспособления
При значительном нарушении двигательной активности ребенку может помочь использование специальных ортопедических приспособлений.

В частности, в результате деформационных процессов в первую очередь страдает мышечная ткань икроножной области, для ее поддержания используются специальные стяжки, которые позволяют ребенку нормально ходить.
Если заболевание имеет ярко выраженную форму, пациент в значительной мере утратил двигательные навыки, ему потребуется правильно подобранное инвалидное кресло.
Причины и признаки дистрофии у ребёнка
Прежде всего, нужно понять, что дистрофия представляет собой патологический процесс, характеризующийся потерей или ненакапливанием полезных веществ в тканях организма. В результате разрушаются клетки и дестабилизируется работа различных органов и систем. Чаще всего дистрофия диагностируется у ребёнка до года или до трёх лет.
Дистрофия у ребёнка может быть следствием следующих ситуаций:
- Генетические врождённые нарушения метаболизма;
- Соматические и хромосомные заболевания ребёнка;
- Стрессовая ситуация и неблагоприятные внешние факторы;
- Неправильное питание: недостаточное, несбалансированное и т.д.;
- Проблемы с пищеварительной функцией организма;
- Нарушение сна ребёнка, пренебрежением режимом дня;
- Инфекционные заболевания у ребёнка;
- Слабая иммунная система малыша;
- Неблагоприятное течение беременности;
- Преждевременные роды и недоношенность плода.
Для того чтобы распознать дистрофию у ребёнка до года, нужно обратить внимание на следующие моменты
- Эмоциональная подвижность ребёнка: повышенная возбудимость и быстрая утомляемость;
- Слабость малыша на фоне потери аппетита и ухудшения сна: беспокойное засыпание, бессонница;
- Потеря веса, недобор по таблице роста и веса детей до года, задержка роста и развития ребёнка.
Многие мамы пытаются решить проблему дистрофии у ребёнка усиленным питанием, однако, это не совсем верный путь. Требуется комплексное лечение, которое назначает врач после детальной диагностики дистрофии.
Медикаментозное лечение дистрофии у детей
Данный вид терапии применяется только в том случае, когда имеется срочная в этом необходимость. Проделывается все для того, чтобы ребенок пришел в норму. Кроме того, благодаря медикаментозному лечению у малыша не должно возникнуть осложнений.
Существует несколько видов данной терапии.
Так, первым из них является пероральное введение пищевых ферментов. Как правило, их назначают сразу же. В этом случае специалист выписывает такие лекарственные средства, как панкреатин совместно с углекислым кальцием либо пепсин с соляной кислотой.
Вторым видом медикаментозной терапии является лечение витамином С и В. Дозы этих полезных веществ при дистрофии у ребенка должны быть выше почти в 6 раз. Такие витамины, как D, А выписываются малышу лишь в случае их недостачи.
Для того чтобы устранить проблемы, связанные с метаболизмом, применяется гормональный метод лечения. Здесь речь идет о таких медикаментах, как “”Неробол”” и “”Тиреоидин””.
Кроме того, в педиатрии при дистрофии у детей для стимуляции организма вводится донорская кровь, а также у-глобулин. Кроме того, в этом случае применяются и ректальные свечи, именуемые “”Апилак””.
При врожденной дистрофии происходит поражение центральной нервной системы. Для того чтобы предотвратить осложнения, специалист выписывает глутаминовую кислоту и уколы “”Церебролизин””.
Родителям следует знать, что данная патология может развиться вследствие наличия камней в желчном пузыре.
Лечение дистрофии у малышей считается сложным и длительным процессом. Поэтому родители должны хорошо смотреть за своим ребенком, а также соблюдать все наставления врача.
Причины дистрофии у детей
Развитие врождённой дистрофии происходит под влиянием негативных факторов, нарушающих полноценное формирование и развитие плода:

- токсикозы беременных;
- возраст матери до 20 или старше 40 лет;
- отсутствие сбалансированного питания, курение и регулярные стрессы во время вынашивания ребёнка;
- работа будущей мамы на вредном производстве с повышенным уровнем шума, вибрациями, а также химическими веществами;
- болезни у беременной женщины (различные хронические инфекционные заболевания, патологии сердца и эндокринной системы);
- нарушения плацентарного кровообращения, патологическое прикрепление плаценты и другие отклонения в течение беременности.
Факторы, провоцирующие развитие приобретённой (постанатальной) дистрофии принято делить на внутренние и внешние.
К внутренним факторам относятся патологические состояния, в результате которых нарушается всасывание и переваривание пищи:
- хромосомные нарушения;
- различные отклонения в физическом развитии;
- патологии эндокринной или центральной нервной системы;
- синдром приобретённого иммунодефицита (СПИД);
- болезни желудочно-кишечного тракта;
- пищевая аллергия;
- наследственные заболевания: лактазная недостаточность (непереносимость белка, содержащегося в молоке и молочных продуктах), целиакия (нарушение усвоения белка, который содержится злаках), муковисцидоз (нарушенная работа внутренних органов, вырабатывающих слизь).
Группу внешних факторов развития дистрофии формируют те обстоятельства, в результате которых ребёнок не получает необходимого для формирования нормального веса объёма питательных веществ, а также которые тем или иным образом тормозят процессы переваривания и усвоения пищи.
1. Пищевой фактор является основной причиной данной формы дистрофии. В случае с маленькими детьми расстройство развивается из-за нехватки грудного молока, неправильного выбора смеси или позднего введения прикорма. У детей более старшего возраста её провоцирует несбалансированный рацион, а также недостаточное количество калорий, белков, жиров или углеводов.

2. Токсический фактор. К ним относятся пищевые интоксикации, неблагоприятное действие плохой экологии, длительный приём лекарств.
3. Социальный фактор
Недостаточное внимание со стороны взрослых или частые ссоры родителей провоцируют стресс и могут вызывать развитие дистрофии
Следует помнить о том, что основной причиной дистрофии у детей является неполноценное питание, которое приводит к недостаточному поступлению питательных веществ и энергии в организм, так называемая алиментарная дистрофия.
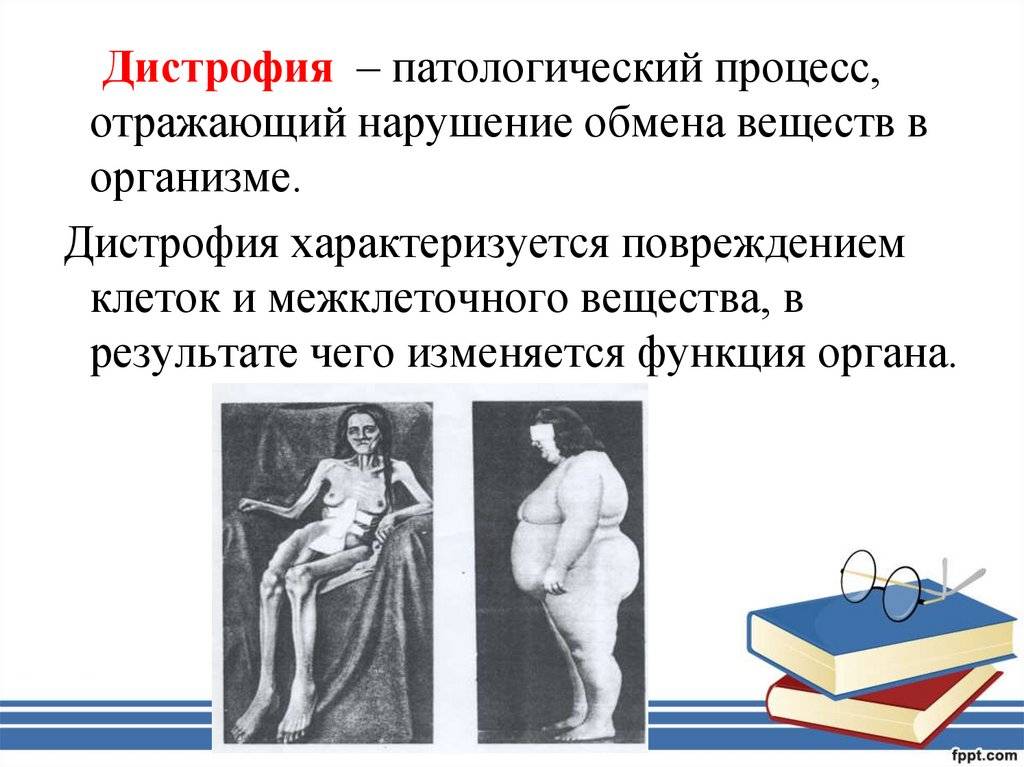
Симптомы дистрофии
Заподозрить дистрофию можно при следующих проявлениях: повышенной возбудимости, утомляемости, ухудшению сна, потери аппетита, снижения веса, у детей – задержке роста. Это общие признаки, которые характеризуют все формы дистрофии. Однако для каждой из них существует особая симптоматика, включающая:
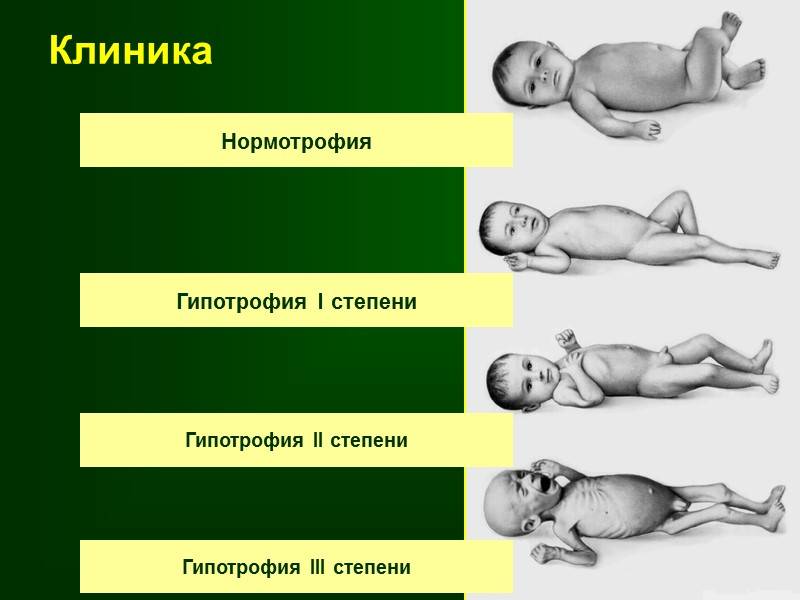
1. Гипотрофия I–II степени: потеря веса на 10-30%, снижение тонуса мышц и эластичности ткани, истончение или исчезновение подкожной клетчатки, бледность кожных покровов, развитие гиповитаминоза, иммунных нарушений, расстройства стула, при которых чередуются запоры и поносы, иногда увеличивается печень.
2. Гипотрофия III степени: значительная потеря веса, снижение эластичности тканей, нарушение дыхания и сердечного ритма, западение глазных яблок, понижение температуры тела и артериального давления.
3. Гипостатура (часто развивается на фоне гипотрофии II–III степени): снижение эластичности тканей, бледность кожных покровов, нарушения метаболизма, расстройства нервной системы и снижение иммунитета. Гипостатура – одна из самых сложных для лечения форм, но если она развивается без остальных симптомов дистрофии, то её можно считать нормальным признаком, сопровождающим конституциональную низкорослость.
4. Паратрофия: избыток жира в подкожной клетчатке, бледность, развитие аллергических реакций, анемия, расстройства кишечника, дисбактериоз, часто наблюдаются опрелости в кожных складках.
Патогенез
Заболевание алиментарной дистрофией может рассматриваться как клиническое выражение нарушенного гомеостаза вследствие непоступления в организм многих пищевых веществ в нужном количестве (см. Голодание). Если потребление пищевых веществ уменьшено, то организм в течение какого-то срока может поддерживать гомеостаз, снизив расход энергии. Это имело место у больных алиментарной дистрофией, у которых, по данным Ю. М. Гефтер, основной обмен снижался до 37%, а по данным Киса, после 24-недельного голодания — до 39%. Возможно, что здесь играет роль изменение гормональной регуляции. В эксперименте было установлено снижение функции гипофиза при голодании животных. В этих же условиях Жиру (P. Giroud) констатировал исчезновение из аденогипофиза эозинофильных клеток. Клинические наблюдения свидетельствуют, что у больных алиментарной дистрофией отмечены отчетливые признаки недостаточной функции ряда эндокринных желез — гипофиза, надпочечников, половых желез, щитовидной железы (М. В. Черноруцкий).
При продолжающемся недостатке питания организм расходует собственные запасы: исчезают жировые депо, используются тканевые белки, жиры и углеводы. Довольно рано отмечается снижение уровня сахара крови, сначала до низших значений нормы, затем до гипогликемического уровня. Особенно низкий уровень сахара крови (25—40 мг%) отмечается во время голодной комы. Содержание холестерина и нейтрального жира в крови также снижается.
Наряду со снижением количественных показателей обмена обнаруживаются и качественные его изменения. Нарастает уровень молочной кислоты, в моче появляются ацетон и ацетоуксусная кислота в повышенном количестве. В более поздние сроки болезни отмечено снижение рН крови.
Особенно выраженные изменения обнаруживаются в белковом обмене. При алиментарной дистрофии отмечается общая гипопротеинемпя, диспротеинемия (нарушение соотношения в крови между содержанием альбуминов и глобулинов в сторону относительного преобладания последних) и происходят глубокие качественные изменения тех функций организма, в реализации которых принимают участие белки. Прежде всего это проявляется нарушением ферментативной деятельности многих, в том числе пищеварительных, желез. Возникшая ферментная недостаточность углубляет состояние дистрофии тканей и органов вследствие нарушения всасывания пищевых продуктов и их усвоения.
Нарушается выработка гормонов клетками эндокринных желез, следствием чего при алиментарной дистрофии является гормональная недостаточность.
Низкое содержание белка в тканевых жидкостях и крови при измененной их белковой структуре является основным фактором в генезе развивающихся отеков. Имеет также значение повышенное введение с пищей хлористого натрия, нарушения гормональной регуляции водно-солевого обмена, замедление тока крови.
При алиментарной дистрофии описаны три вида наступления летального исхода (М. В. Черноруцкий): медленное постепенное умирание, когда больной длительное время находится как бы на грани жизни и смерти; ускоренная смерть и мгновенная смерть.
Второй вид, когда умирание продолжается не больше суток, характерен для больных алиментарной дистрофией,осложненной инфекционной болезнью, которая была непосредственной причиной смерти больного. Внезапная смерть наступала в момент какого-нибудь, подчас ничтожного напряжения (еда, попытка встать с кровати и тому подобное). Во всех случаях смерти играет роль крайнее истощение нейро-эндокринной системы, в частности диэнцефало-гипофизарных отделов, вызванное голоданием и длительным перенапряжением нервных клеток.
На высоте развития А. д. в блокированном Ленинграде совершенно исчезли болезни аллергического генеза: ревматический полиартрит, острый гломерулонефрит, бронхиальная астма. Уменьшилась частота атеросклеротических заболеваний — грудной жабы, инфаркта миокарда. Исчезли приступы почечнокаменной и желчнокаменной болезни. С другой стороны, увеличилось число больных язвенной болезнью и особенно гипертонической болезнью, участились туберкулез, бронхопневмонии, кишечные инфекции.
Структура заболеваемости менялась за время блокады города несколько раз, что указывало на происходящие глубокие изменения реактивности организма под влиянием менявшихся условий жизни и питания населения.
Симптомы дистрофических заболеваний сетчатки
Симптомы заболеваний могут отличаться друг от друга в зависимости от локализации патологического процесса. Перечислим общие признаки, характерные для всех форм заболевания:
- пятно перед глазами;
- ухудшение остроты зрения;
- затруднение ориентировки при неярком освещении;
- потеря или ослабление бокового (периферического) зрения;
- искажение или нечеткое видение очертаний предметов.
Дистрофические заболевания сетчатки: формы, диагностика и лечение

Дистрофические заболевания сетчатки: формы, диагностика и лечение
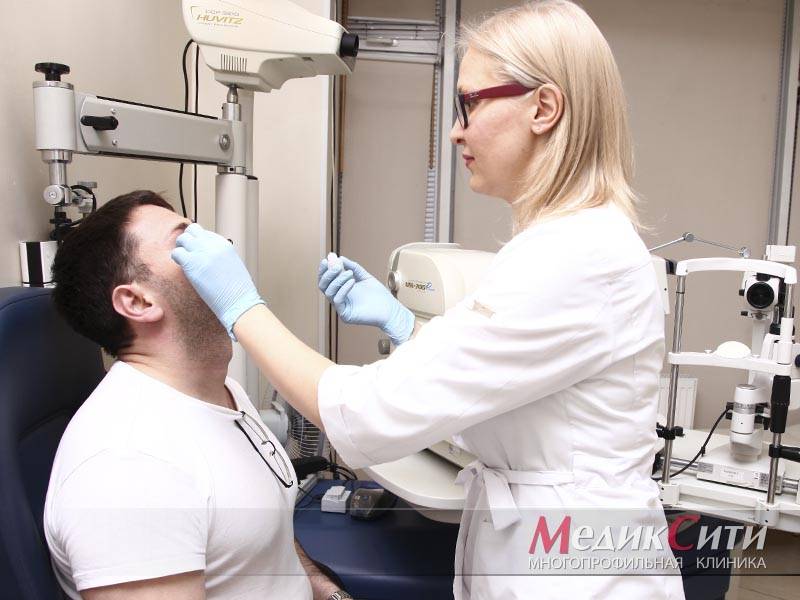
Дистрофические заболевания сетчатки: формы, диагностика и лечение
Периферическая дистрофия сетчатки
Периферическая дистрофия сетчатки на ранней стадии заболевания симптомов не имеет. Пациента может только беспокоить появление «мушек» перед глазами.
Даже офтальмолог не всегда способен выявить патологические процессы, поскольку осмотр глазного дна может не показать появление дистрофических изменений в периферической части. Для этого необходимо обследование глазного дна в условиях мидриаза с широким зрачком и специальная аппаратура.
Клиника «МедикСити» оснащена уникальным прибором для ранней диагностики заболеваний глаз – аппаратом Spectralis HRA+OCT. Применение методов когерентной томографии и флюоресцентной ангиографии помогает выявить начальные изменения в сетчатке и дает точную информацию обо всех структурах сетчатки и зрительного нерва.
Обычно люди, страдающие данной патологией, приходят к офтальмологу только при появлении «пелены» перед глазами. Этот симптом свидетельствует о том, что у человека началось отслоение центральных отделов сетчатки, и восстановить зрение на данном этапе достаточно сложно. Часто патология выявляется в результате стремительно растущей миопии.
Центральная дистрофия сетчатки
В группу центральной дистрофии сетчатки входят несколько заболеваний, которые отличаются характером повреждения и особенностями протекания воспалительного процесса.
Одна из самых распространенных форм — возрастная (макулярная) дегенерация сетчатки глаза. Если не поражаются периферические отделы, то эта форма не приводит к слепоте. При центральной дистрофии сетчатки появляется «раздваивание» предметов, нечеткое и искривленное изображение. Более подробно об этом заболевании (и о сухой и влажной форме) вы можете посмотреть здесь.
Другое распространенное заболевание – центральная серозная хориоретинопатия (ЦСХРП). Появляется после мельчайшего разрыва пигментного слоя сетчатки, что вызывает попадание туда жидкости. Может привести к отслойке сетчатой оболочки глаза. Человек, страдающий ЦСХРП, обладает расплывчатым зрением и видит все предметы в искаженной форме.
Стратегии терапии при дистрофии
Стратегии терапии при дистрофии зависят от типа и причины заболевания. Некоторые общие стратегии включают:
- Физическая терапия и упражнения для укрепления мышц и улучшения подвижности.
- Изменение питания для обеспечения достаточного количества белка, витаминов и минералов, необходимых для роста и развития мышц.
- Хирургические вмешательства для исправления деформаций и улучшения функциональности.
- Применение лекарственных препаратов для улучшения мышечной функции и снижения боли.
- Использование медицинских устройств, таких как ортезы, для поддержки и улучшения функциональности поврежденного сустава или конечности.
- Психологическая поддержка и консультирование для помощи в преодолении эмоциональных и социальных проблем, связанных с дистрофией.
- Генетическое консультирование для семей, которые могут иметь риск наследования дистрофии.
В целом, лечение дистрофии является комплексным и может включать в себя комбинацию различных стратегий.
Лечение
 Схема лечения зависит от формы и степени дистрофии. Она должна включать комплекс мер, которые состоят из применения медикаментозных средств и диетотерапии.
Схема лечения зависит от формы и степени дистрофии. Она должна включать комплекс мер, которые состоят из применения медикаментозных средств и диетотерапии.
При 1 степени гипотрофии допускается терапия в домашних условиях. Перед этим больного необходимо обследовать, выяснить переносимость у него определенных видов продуктов.
Основой терапии дистрофии должна стать коррекция питания. Ее осуществляют путем расчета продуктов на должный вес. Используется принцип «омолаживания» диеты. То есть больного кормят чаще, чем положено по норме и небольшими порциями.
Постепенно объем и энергетическая ценность потребляемых продуктов корректируется. При этом проводят постоянный контроль диуреза, характера стула и других параметров. Лучше завести специальный дневник, и записывать туда все изменения, а также количество и качество употребляемых продуктов.
При гипотрофии 2 и 3 степени необходима разгрузка по объему пищи и по ее содержанию. Разгрузка необходима для восстановления водно-электролитного баланса, функциональности органов, выведения веществ, накопленных вследствие нарушения обменных процессов. Недостаток объема пищи компенсируют парентеральным введением аминокислот, глюкозы, белка и других компонентов.
Лечение тяжелых форм гипотрофии проводится в стационаре. Желательно поместить больного в бокс, создать в нем оптимальный микроклимат (температура +27-30оС, влажность 60-70%), убрать лишние раздражители (звук, свет и т.д.).
Медикаментозные средства
С первого дня лечения назначается прием ферментов в течение 2-3 недель:
- Мезим;
- Креон;
- Панкреатин;
- Фестал.
При тяжелой гипотрофии внутривенно вводят:
- Альвезин;
- Левамин;
- Альбумин.
Чтобы обеспечить окислительно-восстановительные процессы, назначают курсы витаминотерапии:
- парентеральное введение витаминов группы В и С;
- внутрь при необходимости витамины А и D.
Гормональная терапия:
- Тиреодинин;
- Неробол;
- Ретаболил;
- Префизон;
Видео на тему: Анорексия? Дистрофия? Комплексное лечение анорексии, дистрофии народными средствами
Дистрофия у детей
Дистрофия у детей (dystrophia; греческий dys- + trophe питание) — патологическое состояние, характеризующее различные проявления хронических расстройств питания. При этом нарушается не только функция пищеварения, но и усвоение питательных веществ тканями и клетками организма, обмен веществ и жизнедеятельность организма, его рост и развитие. Особенности обмена веществ (смотри полный свод знаний Обмен веществ и энергии, у детей) и реактивности детского организма (смотри полный свод знаний Реактивность организма, у детей) создают условия для возникновения дистрофических состояний у детей раннего возраста при воздействии даже слабых вредных агентов.
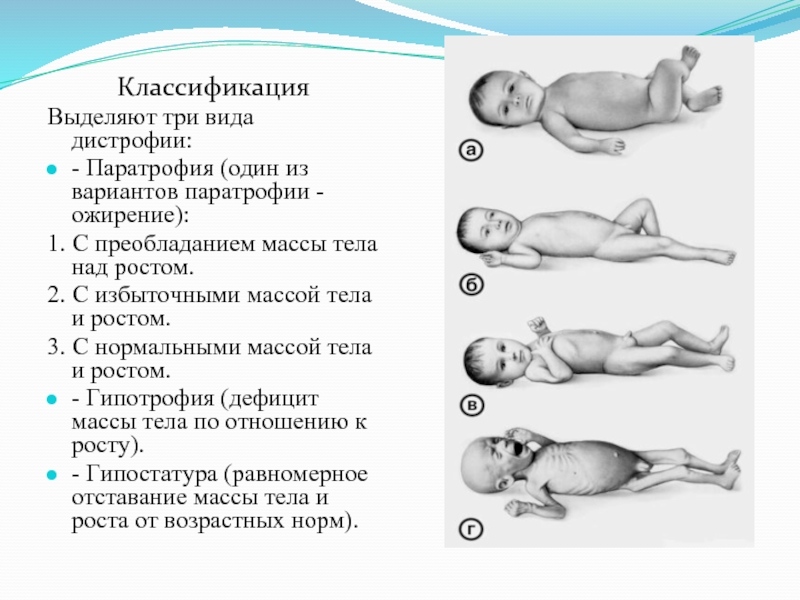
Классификация. По классификации Г. Н. Сперанского и А. С. Розенталь, предложенной в 1945 год, выделяют три типа Дистрофия: гипотрофия (смотри полный свод знаний), гипостатура (смотри полный свод знаний) и паратрофия (смотри полный свод знаний). Г. И. Зайцева и Л. А. Строганова в 1969 год внесли дополнения в данную классификацию, выделив тип, степень тяжести (I, II, III), время возникновения (Дистрофия пренатального, постнатального и смешанного происхождения), период течения (начальный, прогрессирования, реконвалесценции), построив её по этиологического признаку (экзогенные, эндогенные, экзогенно-эндогенные)
Внимание педиатров привлекают Дистрофия пренатального происхождения, которые проявляются с первых дней жизни ребёнка и характеризуются отставанием его в физ. развитии
Данный вид Дистрофия обсуждается в отечественной и зарубежной литературе под разными названиями — Дистрофия новорожденных, Дистрофия при рождении, низкий вес при рождении, внутриутробная гипотрофия, врождённая гипотрофия и так далее (доклад Комитета экспертов ВОЗ, 1961 год). Тяжёлые формы внутриутробных гипотрофий называют нейродистрофиями, подчёркивая их центральный генез.
Этиология и патогенез
В возникновении Дистрофия у детей имеют значение экзогенные и эндогенные факторы. К экзогенным относятся: алиментарный (недокорм, качественное нарушение состава пищи, преобладание в ней углеводов при малом количестве белка и жира, недостаток витаминов), инфекционный (дизентерия, пневмония и другие) и токсический факторы, а также погрешности в уходе за ребёнком (нарушение гигиенических режима, отсутствие установленного режима дня и так далее). Среди эндогенных причин имеют значение аномалии конституции ребёнка, эндокринные и нейроэндокринные расстройства, пороки развития различных органов и систем (центральная нервная система, сердечно-сосудистой системы, желудочно-кишечного тракта, почек, лёгких и так далее), наследственные нарушения обмена веществ — аминокислотного, углеводного, жирового, например, синдром мальабсорбции (смотри полный свод знаний Мальабсорбции синдром), галактоземия и другие
Патогенез Дистрофия сложен. Наблюдается понижение возбудимости головного мозга и нарушается регуляторная деятельность центральная нервная система, что влияет на функции желудочно-кишечного тракта (нарушается всасывание белков, жиров и витаминов), снижается ферментативная энергия крови, изменяются процессы усвоения питательных веществ тканями и клетками организма. Развивается расстройство питания и всех видов обмена. Организм для поддержания жизнедеятельности использует белки, жиры и углеводы собственных тканей, что приводит к истощению.
В формировании внутриутробных Дистрофия большое значение имеет питание во время беременности (смотри полный свод знаний Беременность, гигиена и питание беременных), которое может быть достаточным по калорийности, но недостаточным или избыточным по содержанию отдельных пищевых ингредиентов. При недостаточном содержании в пищевом рационе матери белка, особенно животного, и некоторых минеральных веществ ребёнок может родиться с отставанием в росте и весе или с достаточным или даже с избыточным весом за счёт безбелковых отёков (смотри полный свод знаний Алиментарная дистрофия). При преобладании в диете женщины углеводов ребёнок рождается крупным за счёт избыточного отложения жира, образующегося из углеводов. Недостаток в питании будущей матери витаминов приводит к рождению ребёнка с признаками гиповитаминоза (смотри полный свод знаний Витаминная недостаточность), а также с отставанием в весе и росте.
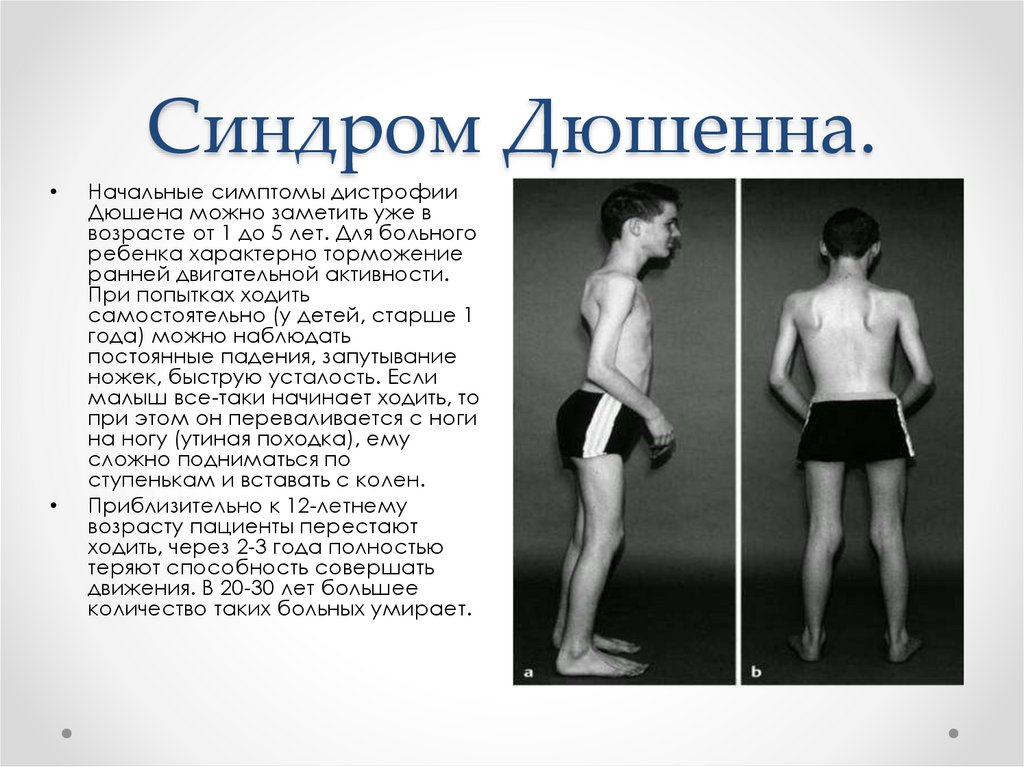
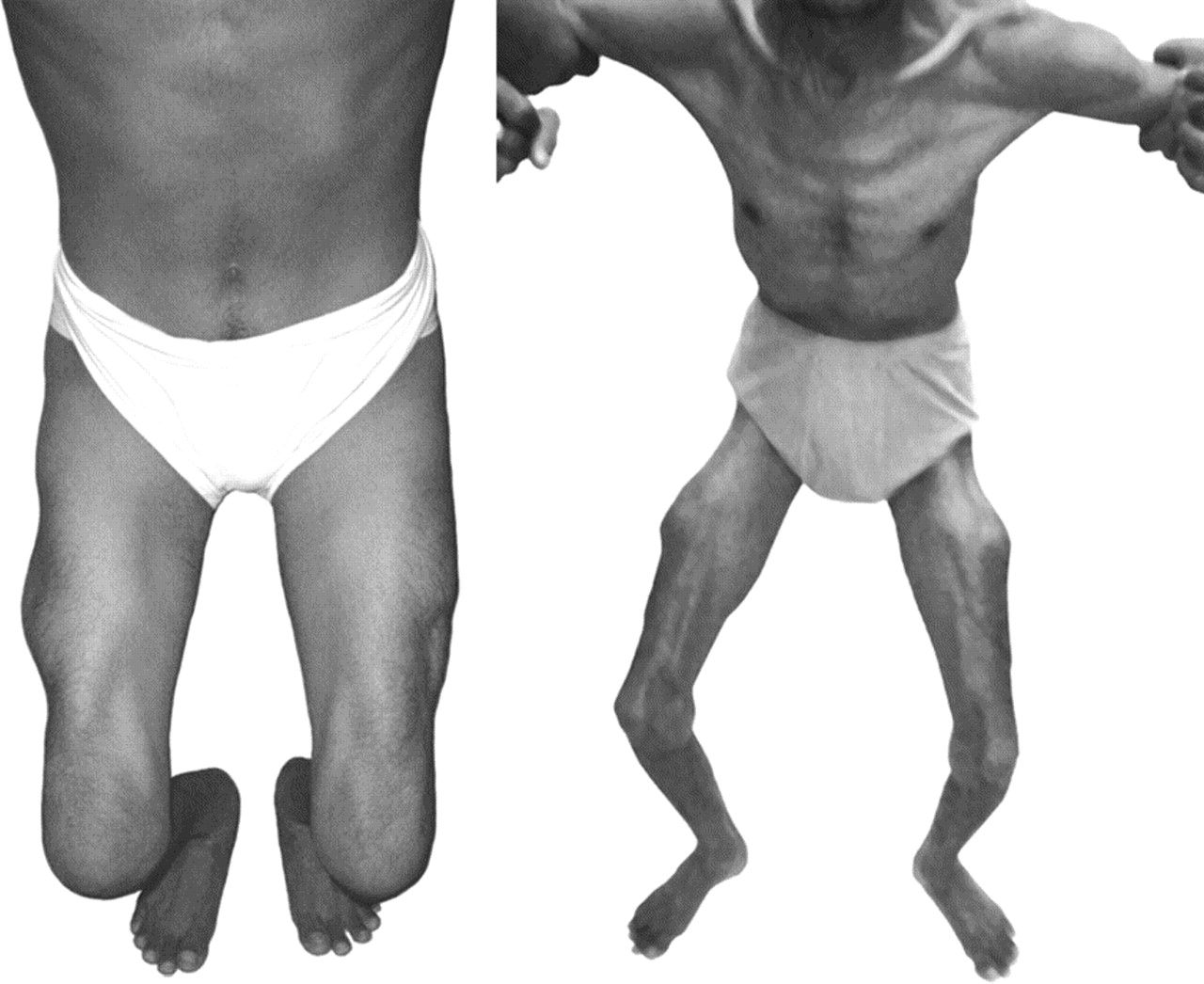
В чем отличие мышечной дистрофии Дюшенна от дистрофии Беккера?
Как дистрофия Дюшенна, так и дистрофия Беккера относятся к категории мышечных дистрофий. Несмотря на это дистрофия Дюшенна встречается в медицинской практике намного чаще дистрофии Беккера. Также дистрофия Дюшенна является еще и намного более опасным заболеванием по сравнению с дистрофией Беккера. Следует отметить еще и то, что оба данных заболевания завладевают мышцами всего тела, вызывая при этом очень сильную слабость мышц, которые располагаются вблизи туловища.
Обе эти дистрофии являются следствием дефектного гена, только дефекты эти в каждом отдельном случае располагаются на отдельных участках Х-хромосомы
Обращаем Ваше внимание на то, что мышечная дистрофия не способна поражать представительниц прекрасного пола, так как в их организмах над дефектным геном берет верх нормальный ген другой Х-хромосомы. Данное заболевание характерно только для мужчин
Если верить статистическим данным, то мышечная дистрофия Дюшенна встречается примерно у двадцати – тридцати процентов новорожденных мальчиков из ста тысяч. Что же касается дистрофии Беккера, то данное заболевание присуще только трем мальчикам из ста тысяч новорожденных.
Если сравнивать сроки проявления данных двух заболеваний, то дистрофия Дюшенна дает о себе знать уже в три – семь лет, а вот дистрофия Беккера может развиться только к десяти годам. Если дети с заболеванием Дюшенна к двадцати годам чаще всего умирают, то дети, больные дистрофией Беккера в двадцать лет еще могут передвигаться в инвалидном кресле самостоятельно. В любом случае, оба данных заболевания являются смертельными.
О профилактических мерах
Для того чтобы избежать врожденной патологии, будущей матери следует вести здоровый образ жизни.
Итак, основами профилактики дистрофии у детей является соблюдение нескольких рекомендаций для девушек в положении. Они должны в обязательном порядке отказаться от чрезмерных физических нагрузок, а также избегать стрессов.
Рацион как будущей мамы, так и уже родившей, должен быть правильным. Под последним подразумевается сбалансированное питание. Благодаря этому и грудное молоко, которым питается малыш, будет насыщено всеми необходимыми полезными веществами.
Перед зачатием детей каждая женщина должна пройти обследование на наличие инфекционных заболеваний. В случае если они имеются, необходимо для начала пройти лечение. При наличии хронических заболеваний следует постоянно посещать специалиста.
Будущей матери категорически запрещается употреблять спиртные напитки, а также курить. А о наркотических веществах и речи быть не может.
Профилактические меры приобретенной формы патологии подразумевают под собой кормление малыша грудным молоком до 1,5 лет. Также прикорм следует вводить вовремя. При искусственном вскармливании малыша необходимо верно подбирать молочную смесь. Как правило, в этом случае необходима консультация специалиста.
Также не стоит забывать о различных методах укрепления иммунитета ребенка.
Заключение
О профилактике данного заболевания нужно задуматься ещё на этапе планирования беременности. Каждой будущей маме необходимо вылечить все имеющиеся острые и хронические заболевания и отказаться от любых вредных привычек.
Уже после рождения ребёнка обязательно соблюдать все правила кормления и ухода за ним, регулярно посещать педиатра и контролировать все антропометрические показатели, а также своевременно лечить заболевания.
Мария Казакова, Врач-неонатолог 52 статей на сайте
По окончании университета прошла интернатуру по направлению «Неонатология» в СамГМУ. После завершения профессиональной подготовки, и по настоящее время, работаю врачом-неонатологом в ГУЗ Городская клиническая больница №1 (Перинатальный центр) г. Ульяновск.